Ang muling pagkabuhay ng mga baterya ng sodium-ion na temperatura sa silid
Dahil sa maraming reserbang sodium (Na) sa crust ng Earth at sa mga katulad na katangian ng physicochemical ng sodium at lithium, ang sodium-based na electrochemical energy storage ay may malaking pangako para sa malakihang pag-iimbak ng enerhiya at pagbuo ng grid. Halimbawa, ang high-temperature zero emission battery research activity cells batay sa Na/NiCl2 system at high-temperature Na-S cells, na matagumpay na komersyal na mga kaso ng stationary at mobile application, ay nagpakita na ng potensyal ng sodium-based rechargeable na mga baterya. Gayunpaman, ang kanilang mataas na operating temperature na humigit-kumulang 300 °C ay nagdudulot ng mga isyu sa seguridad at nagpapababa sa round-trip na kahusayan ng mga sodium-ion na baterya (SIB). Kaya naman malawak na itinuturing ang mga Room-temperature (RT) SIB bilang ang pinaka-promising na alternatibong teknolohiya sa LIB.
Sa kasaysayan ng mga baterya sa nakalipas na 200 taon, ang pananaliksik sa mga SIB ay taimtim na isinagawa nang magkatabi sa pagbuo ng LIB. Ang aktibidad ng electrochemical ng TiS2 para sa lithium at ang pagiging posible nito para sa pag-iimbak ng enerhiya ay unang iniharap noong 1970s. Kasunod ng pagtuklas na ito, ang kakayahan ng mga Na ions na maipasok sa TiS+2 ay natanto noong unang bahagi ng 1980s. Sa pagkatuklas ng graphite bilang mura at katamtamang kapasidad na anode na materyal para sa mga LIB at ang pagkabigo na mag-intercalate ng mga sodium ions, ang mabilis na pag-unlad ng LIB ay naganap noong 1990s, na pinalitan ang paglaki ng sodium chemistry. Pagkatapos, noong 2000, ang pagkakaroon ng sodium storage sa hard carbon (HC), na maghahatid ng kapasidad ng enerhiya na katulad ng sa Li sa graphite, nagpabata ng interes sa pananaliksik sa mga SIB.
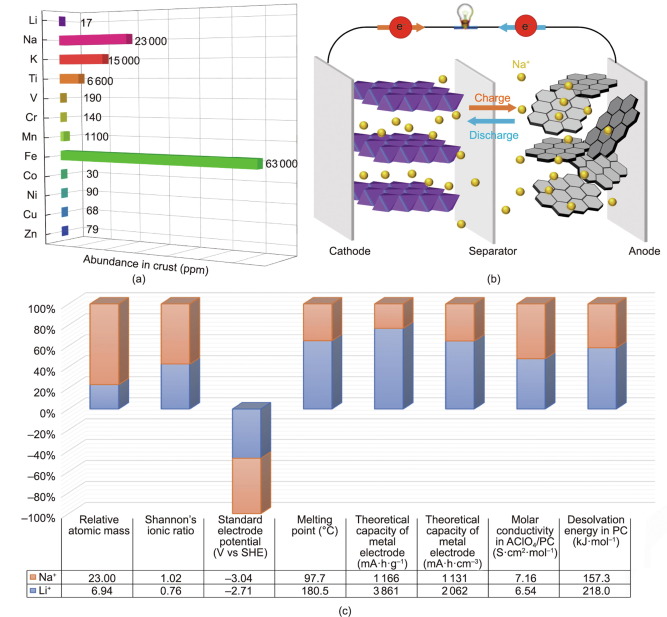
Isang paghahambing ng baterya ng Sodium-ion at baterya ng Lithium-ion
Ang muling pagkabuhay ng mga SIB—kasama ang patuloy na pagtaas ng presyon mula sa kakulangan ng pagkakaroon ng mga reserbang lithium at ang katumbas na pagtaas ng gastos—ay nagbibigay ng pantulong na diskarte sa mga LIB. Ang mga SIB ay nakakuha ng pagtaas ng pansin sa pananaliksik, kasama ng mga pangunahing tagumpay sa agham ng mga materyales, sa pagnanais na masiyahan ang pagtaas ng pagtagos ng mga teknolohiyang nababagong enerhiya. Ang mga sangkap ng cell at ang mga mekanismo ng reaksyon ng electrochemical ng mga SIB ay karaniwang magkapareho sa mga LIB, maliban sa carrier ng singil, na Na sa isa at Li sa isa. Ang pangunahing dahilan para sa mabilis na pagpapalawak sa kimika ng mga materyales ng SIB ay ibinibigay sa mga parallel sa mga katangian ng physicochemical sa pagitan ng dalawang metal na alkali.
Una, ang mga prinsipyo ng pagpapatakbo at pagbuo ng cell ng mga SIB ay katulad ng sa mga komersyal na LIB, kahit na may Na nagsisilbing tagadala ng bayad. Apat na pangunahing bahagi ang umiiral sa isang tipikal na SIB: isang cathode material (karaniwan ay isang Na-containing compound); isang materyal na anode (hindi kinakailangang naglalaman ng Na); isang electrolyte (sa isang likido o solid na estado); at isang separator. Sa panahon ng proseso ng pagsingil, ang mga sodium ions ay kinukuha mula sa mga cathode, na karaniwang mga layered na metal oxide at polyanionic compound, at pagkatapos ay ipinasok sa mga anod, habang ang kasalukuyang naglalakbay sa pamamagitan ng isang panlabas na circuit sa kabaligtaran ng direksyon. Kapag naglalabas, ang Na ay umaalis sa mga anod at bumabalik sa mga cathode sa isang proseso na tinutukoy bilang "ang prinsipyo ng rocking-chair." Ang mga pagkakatulad na ito ay nagbigay-daan sa paunang pag-unawa sa at mabilis na paglago sa teknolohiya ng SIB.
Bukod dito, ang mas malaking ionic radius ng Na ay nagdudulot ng sarili nitong mga pakinabang: nadagdagan ang flexibility ng electrochemical positivity at nabawasan ang de-solvation energy sa polar solvents. Ang mas malaking agwat sa ionic radius sa pagitan ng Li at ang transition metal ions ay kadalasang humahantong sa pagkabigo ng flexibility ng materyal na disenyo. Sa kaibahan, ang isang sodium-based na system ay nagbibigay-daan sa mas nababaluktot na solidong istruktura kaysa sa isang lithium-based na sistema, at nagtataglay ng napakalaking ionic conductivity. Ang isang tipikal na halimbawa ay ang β-Al2O3, kung saan ang Na intercalation ay may perpektong sukat at mataas na conductivity. Ang mas maraming layered transition metal oxides na may iba't ibang M+x+ stacking manners ay madaling ma-realize sa isang sodium-based system. Katulad nito, ang malawak na pagkakaiba-iba ng mga istrukturang kristal na kilala para sa pamilya ng sodium ionic conductor (NaSICON) ay mas kumplikado kaysa sa mga analog na lithium. Higit sa lahat, ang isang mas mataas na ionic conductivity ay maaaring pahintulutan sa NaSICON compound, na higit na lumampas sa ionic conductivity sa lithium ionic conductor (LiSICON) compound.
Panghuli ngunit hindi bababa sa, ang mga sistematikong pagsisiyasat na may iba't ibang mga aprotic polar solvents ay nagpakita na ang mas malaking ionic radius ng Na ay nagdudulot ng mas mahinang desolvation energy. Ang mas maliit na Li ay may mas mataas na surface charge density sa paligid ng core kaysa sa Na kapag pareho silang nagtataglay ng parehong valence. Ang Li ay samakatuwid ay thermodynamically nagpapatatag sa pamamagitan ng pagbabahagi ng higit pang mga electron sa mga polar solvent molecule. Iyon ay, ang Li ay maaaring mauri bilang isang uri ng Lewis acid. Bilang isang resulta, ang isang medyo mataas na enerhiya ng desolvation ay kinakailangan para sa mataas na polarized Li, na humahantong sa isang medyo malaking paglaban sa paglipat na sapilitan ng transportasyon ng Li mula sa likidong estado (electrolyte) patungo sa solidong estado (electrode). Dahil malapit na nauugnay ang desolvation energy sa mga transfer kinetics na nagaganap sa liquid/solid interface, ang relatibong mababang desolvation energy ay isang makabuluhang bentahe para sa pagdidisenyo ng mga high-power na SIB.